
来源:财经报道网
2026-03-25 17:36:05
(原标题:君赛生物创新GC101 TIL疗法,国内率先开启针对NSCLC的II期临床)
2026年3月25日-3月28日,由欧洲肿瘤内科学会(ESMO)与国际肺癌研究协会(IASLC)联合主办的2026 欧洲肺癌大会(ELCC)将于丹麦哥本哈根盛大举行。
作为全球肺癌领域最具影响力的国际学术会议之一,ELCC汇聚全球胸部肿瘤领域顶尖专家,是业内交流前沿科研进展、临床数据和教育实践的重要平台。
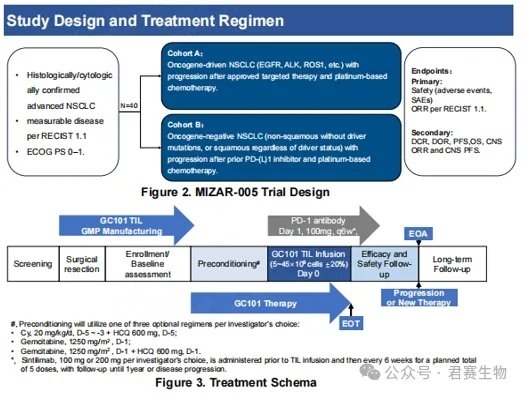
本届大会上,君赛生物将正式公布“自体天然肿瘤浸润淋巴细胞注射液(GC101)治疗晚期非小细胞肺癌(NSCLC)Ib期临床试验(MIZAR-005)”研究方案。
MIZAR-005(NCT06473961)是一项Ib期、开放标签、单臂临床试验,旨在评估GC101 TIL细胞注射液在晚期NSCLC的安全性和疗效。研究主要终点为安全性和客观缓解率(ORR),次要终点涵盖疾病控制率(DCR)、缓解持续时间(DOR)、无进展生存期(PFS)和总生存期(OS)等关键指标。
GC101治疗肺癌的II期临床试验正式启动
基于Ib期临床试验的探索成果与安全性验证,君赛生物正式推进GC101治疗晚期NSCLC的 II 期临床研究。MIZAR-005项目目前已在组长单位上海交通大学附属胸科医院、湖南省肿瘤医院等全国多个分中心相继启动开展。
肺癌是中国发病率和死亡率最高的恶性肿瘤。非小细胞肺癌(NSCLC)占肺癌患者的80%-85%,约70%的患者确诊时已处于疾病晚期,5年生存率仅为15%。尽管TIL疗法在实体瘤治疗中已展现出良好前景,但传统TIL疗法依赖高强度清淋化疗及大剂量IL-2给药,不良反应突出是制约其广泛应用的核心痛点。
针对TIL疗法的行业瓶颈,君赛生物自主开发全球首款无需高强度清淋化疗、无需IL-2给药的创新型天然TIL疗法GC101。该疗法在Ⅰ期临床研究中已展示出优异的疗效与良好的安全性:数据显示,针对中位前序治疗三线的晚期患者,GC101实现41.7%客观缓解率(ORR)与66.7%疾病控制率(DCR),12个月总生存率为66.7% (95% CI: 33.7%, 86.0%)。中位随访时间13.0个月(范围:1.5-31.1),中位总生存期尚未达到。

“晚期NSCLC的靶向和免疫疗法近年来取得不错的进展,但依然存在诸如克服耐药机制和解决肿瘤异质性等挑战。对于晚期NSCLC,一线治疗失败后,免疫治疗与化疗带来的获益有限,临床上仍存在对安全性更高、疗效更持久的细胞疗法的未满足需求。
君赛生物GC101前期的临床试验数据向我们展示了颇具前景的疗效,期待进一步发现TIL疗法在治疗NSCLC患者的潜力。希望这款创新TIL疗法能够造福更多肺癌患者,切实提升患者生命质量。”
关于GC101
GC101依托君赛生物自主开发的DeepTIL细胞富集扩增平台开发而成,是君赛生物研发进度最快的TIL疗法管线,也是全球首款无需高强度清淋化疗、无需IL-2给药的天然TIL疗法。
临床数据显示,GC101已为多线治疗失败的晚期转移性实体瘤患者带来长期获益,包括黑色素瘤、非小细胞肺癌、宫颈癌、子宫内膜癌、脑胶质瘤、胰腺癌等类型的肿瘤患者在接受GC101治疗后,展现客观缓解疗效,无瘤生存最久已超4年。
关于MIZAR-005临床试验
MIZAR-005临床试验项目已在上海交通大学附属胸科医院、湖南省肿瘤医院等医疗机构进行受试者招募及筛选,招募主要标准如下。
主要入组标准:
1、18-75岁,男女不限;
2、经细胞学或组织病理学诊断明确的晚期非小细胞肺癌患者;
3、经过靶向及含铂双药化疗治疗失败,或经PD-(L)1联合含铂化疗治疗失败;4、有可取材的肿瘤病灶用来生产TILs,且能接受相关取材手术;
5、ECOG评分0-1分;
6、有足够的血液学和终末器官功能。
主要排除标准:
1、有严重基础性疾病;
2、有重大传染性疾病;
3、肺纤维化、间质性肺病、急性肺病;
4、脑转移不稳定或伴有临床症状。
本文来源:财经报道网
时代财经
2026-03-25
财经报道网
2026-03-25
财经报道网
2026-03-25
财经报道网
2026-03-25
财经报道网
2026-03-25
财经报道网
2026-03-25
证券之星资讯
2026-03-25
证券之星资讯
2026-03-25
证券之星资讯
2026-03-25

